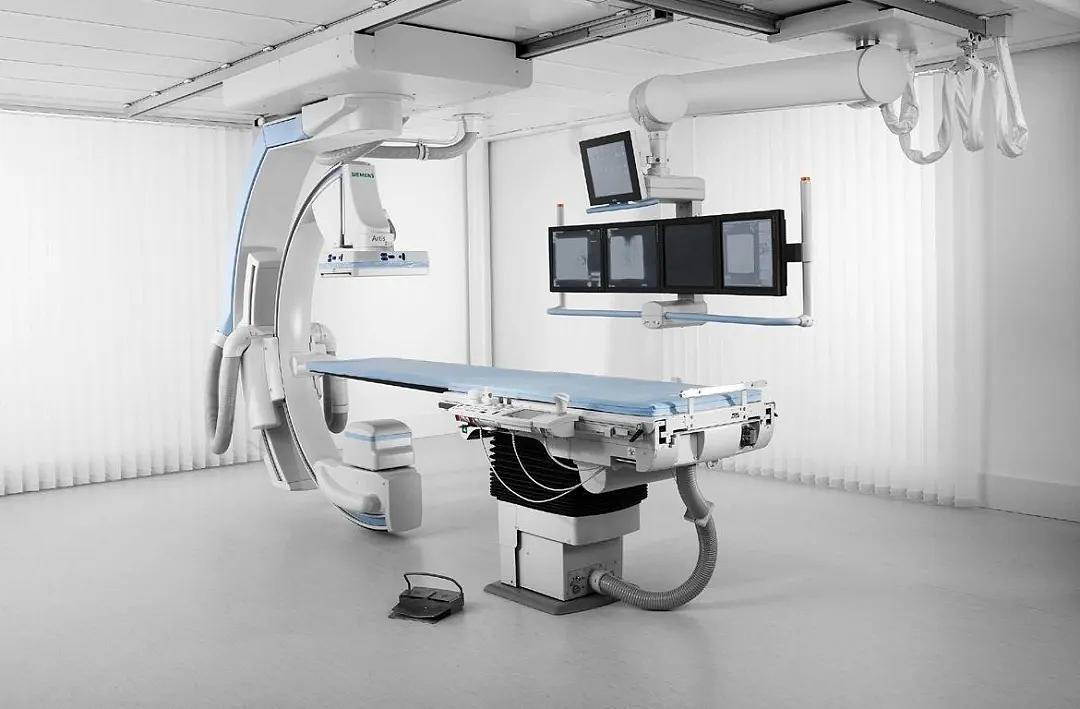
市场和质量监督管理局:药品、医疗器械监督销毁
类别:政策法规 作者:画明环境发布时间:2021-05-01 16时 浏览人次:1.72 K
药品、医疗器械监督销毁
| 类别 | 行政检查 | ||
| 实施主体 | 市场和质量监督管理局 | 行使层级 | 本级保留 |
| 实施依据 | 《麻醉药品和精神药品经营管理办法(试行)》第四十条:企业对过期、损坏的麻醉药品和精神药品应当登记造册,及时向所在地县级以上药品监督管理部门申请销毁。药品监督管理部门应当自接到申请起5日内到现场监督销毁。 《中华人民共和国药品管理法》第四十二条:国务院药品监督管理部门对已经批准生产或者进口的药品,应当组织调查;对疗效不确、不良反应大或者其他原因危害人体健康的药品,应当撤销批准文号或者进口药品注册证书。 已被撤销批准文号或者进口药品注册证书的药品,不得生产或者进口、销售和使用;已经生产或者进口的,由当地药品监督管理部门监督销毁或者处理。” 《生物制品批签发管理办法》第三十三条“属于本办法第三十条、第三十一条情形的,已上市销售的生物制品,应当责令药品生产企业收回,并按照有关规定在(食品)药品监督管理部门的监督下予以销毁。 《医疗器械召回管理办法(试行)》 第二十一条:医疗器械生产企业对召回医疗器械的处理应当有详细的记录,并向医疗器械生产企业所在地省、自治区、直辖市药品监督管理部门报告。对通过警示、检查、修理、重新标签、修改并完善说明书、软件升级、替换、销毁等方式能够消除产品缺陷的,可以在产品所在地完成上述行为。需要销毁的,应当在销毁地药品监督管理部门监督下销毁。 | ||
| 备注 | |||
下一篇:焚烧销毁处置 上一篇:医疗器械销毁步骤流程是什么样的?